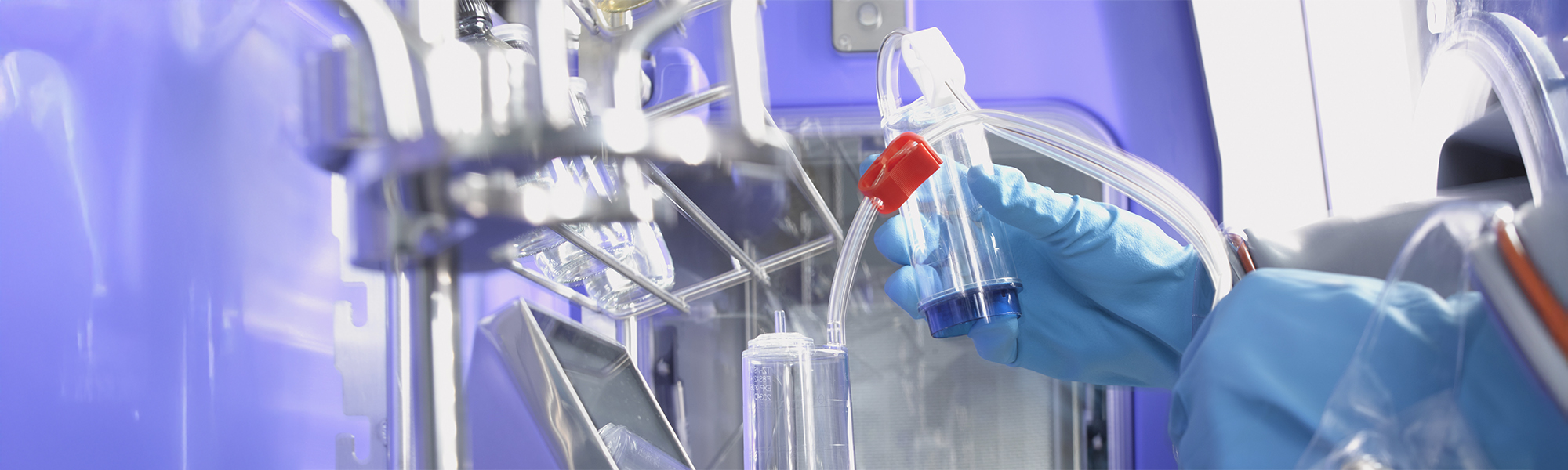
保护无菌检测过程的重要性
在整个生产过程中都需要采集产品样品,并对其进行微生物污染检测。在大多数情况下,无菌检测都将证明产品没有受到污染,从而允许产品出货。一旦检测结果显示产品受到污染,即会停止发货,以防止给患者带来潜在风险。
如果您的无菌过程未能得到适当保护,来自环境的污染就可能影响检测结果,导致未被污染的产品显示受到污染。这会给生产商带来巨大的成本,而且如果这批药品不得不报废,还可能造成患者药品短缺问题。帮助保护无菌检测过程避免周围环境的污染,可以降低假阳性的风险。
无论是膜过滤法,还是直接接种法,隔离器都可以提供明显的优势。

了解我们的无菌检测隔离器
艺康Bioquell Qube提供无菌ISO 5/A级环境,包括集成的Bioquell过氧化氢蒸汽*技术,可在操作区域的暴露表面实现经过验证的6-log的孢子杀灭率。从聚合物成型工艺到与Merck Millipore Symbio Flex无菌泵的集成,Bioquell Qube确实是无菌检测独一无二的理想解决方案。
*按照标签说明使用时,艺康Bioquell系统使用Bioquell过氧化氢消毒剂-AQ(EPA注册号:1677-277)
隔离器是您的正确选择吗?您拥有适当的隔离器吗?
假阳性问题对您有什么影响?
由于假阳性而停止生产可能导致长时间停产、不必要的产品报废、药物短缺,并可能降低企业在市场上的地位。此外,CAPA相关措施所带来的额外时间、人工和成本也需要加以考虑。
这个过程需要多少洁净室空间?
洁净室空间通常需要加以优化,因为单位面积洁净室的建造和运行成本相当昂贵。像Bioquell Qube这样的隔离器占地面积小,甚至可以根据需要轻松移动,无需施工作业,而且可以在较低等级的区域运行。如需了解具体规格,请联系艺康。
您的无菌检测过程需要B级洁净室吗?
使用隔离器,您可以在较低级别的洁净室进行检测,对净化服的要求更低,甚至无需穿着净化服。此外,宝贵的洁净室空间可以留作其他关键操作之用,而且有助于降低运营成本,因为更高级别的洁净室需要在能源和维护成本方面投入更多资金。
您目前的过程是否经过验证并真正可重复?
进料的自动生物净化是一个经过验证的过程,可确保每个循环都具有相同的功效。因此,这可以进一步帮助降低假阳性的风险。
您一天需要做多少次无菌检测?
洁净室空间通常需要加以优化,因为单位面积洁净室的建造和运行成本相当昂贵。像Bioquell Qube这样的隔离器占地面积小,甚至可以根据需要轻松移动,无需施工作业,而且可以在较低等级的区域运行。根据具体的配置,Bioquell Qube每天最多可完成60项检测。如需了解具体规格,请联系艺康。
您是否外包您的无菌检测过程?
将检测过程引入内部具有诸多优势,包括对过程拥有更多的控制、长期成本节约以及更快获得检测结果。选择一种可以放置在受控无分类(CNC)区域或较低级别洁净室的隔离器即可使之成为现实,尽管这会产生一笔前期设备相关费用。

检测不合格的后果
检测不合格会对药品制造商造成巨大的影响,因为这通常会导致:
- 拒绝产品放行并可能报废未通过检测的同批次产品
- 对生产区域进行额外的清洁和消毒
- 监管介入
- 制造商的经济损失
- 及时进行调查
- 患者药品短缺
- 在调查期间停止后续产品的生产
然而,无菌检测不合格并非总是由产品污染引起的。
当来自环境或检测操作人员的污染进入检测过程,导致检测不合格时,即会出现假阳性。产品将被视为受到污染,但实际上并不含有害微生物。
在无菌检测不合格的情况下,如要证明不合格是由操作人员和/或实验室环境的污染造成的,其举证责任在制造商身上,这是很难证明的。因此,假阳性常常导致合规、有效的产品被不必要地报废。
利用无菌检测隔离器保护您的生产

有关隔离器的监管指引:
- EU GMP附件1第10.6节指出:
“无菌检测应在无菌条件下进行”
- FDA有关采用无菌工艺生产无菌药品的行业指引更进一步,在第XI节指出:
“使用隔离器进行无菌检测有助于最大限度地降低检测结果出现假阳性的可能性”
- 根据EU GMP附件1,隔离器是指:
“能够进行可复制的内部生物净化的封闭空间,其内部工作区符合A级条件,而且其内部与外部环境能够完全、持续地隔离”

隔离器具备一系列功能来保护无菌过程,包括:
- 所有门上都有气密/充气密封
- 联锁装置可在达到无菌条件后(经过生物净化后)防止门被打开
- 单向气流保持在0.36-0.45 m/s之间(符合EU GMP附件1指导值)
- 采用HEPA过滤器净化进入的空气
- 压差、外壳和手套压力测试分别进行
- 通过环境监测系统来确认环境在使用期间保持无菌
- 气流和压力报警
- 过氧化氢蒸汽生物净化系统可达到6-log的孢子杀灭率*,可消除封闭空间表面以及检测过程所需进料的污染
*按照标签说明使用时,艺康Bioquell系统使用Bioquell过氧化氢消毒剂-AQ(EPA注册号:1677-277)
隔离器的优点
首先,隔离器可以减少无菌检测发生假阳性的风险,通过减少不必要的产品报废,为无菌产品制造商节省数百万美元。
此外,隔离器还可以节省大量运行成本。
与生物安全柜(BSC)/层流罩(LAF)必须位于B级洁净室不同,隔离器可以位于较低的C/D级洁净室。这可以大幅节省开支,包括:
- 低功率HVAC系统可降低能源支出
- 减少清洁和消毒工作所需的人力资源
- 减少洁净室的维护
- 降低清洁消毒耗材成本
- 降低净化服要求
- 提高操作人员的效率(较低的净化服要求意味着他们可以工作更长时间)
1Costing a Cleanroom Per Square Foot, Cleanroom Technology, 28 February 2018
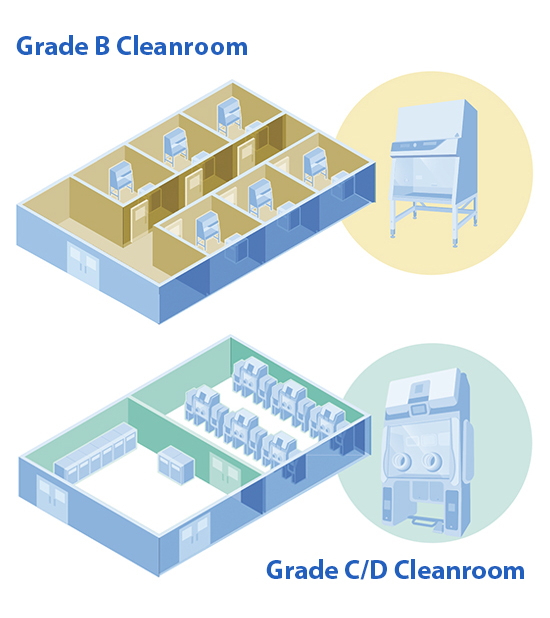

比较传统不锈钢隔离器与Bioquell Qube