外观清洁:澄清法规指导方针
作者:Thomas Altmann,清洁验证全球CIP/COP技术经理

几乎所有制药相关法规(FDA、PIC/S、GMP)中都用到了“外观清洁”一词。简而言之,制药业生产中使用的设备在使用之前都必须进行外观清洁度检查1。
这项要求合乎情理,但是很少有法规100%明确说明了外观清洁在标准操作程序中是指什么,以及如何记录以用于清洁验证。最常见的问题包括:
- 残留物是什么样的?
- 什么是视觉阈值?
- 结构材料如何影响外观?
- 检查员应多久接受一次视力测试?
下面对上述问题分别进行了简短的讨论。
残留物是什么样的?
您的检查员在检查设备时需要知道所要寻找的是什么。他们最好能够区分工艺流程残留物与清洁剂和消毒产品的残留物,以及每种类型的残留物的各种残留量在外观上的区别。此外,检查员还必须知道外观清洁的表面是什么样子,包括钢的染色、划痕以及不影响后续生产步骤的其他损伤。
例如,活性药物成分(API)往往呈粉末状,而洗涤剂残留物则表现为表面上的小点。

API残留物往往呈粉末状。

洗涤剂残留物往往呈小点状。
检查员确定“外观清洁”时经常会遗漏洗涤剂残留物。使用专为食品饮料应用设计的洗涤剂的药品制造商应注意到,缓蚀剂和特定的表面活性剂等非水溶性成分的残留物可能会继续留在表面上,并与API的残留物产生意外的相互作用,而且有可能转移到后续生产的产品中。
结构材料如何影响外观?
残留物的外观可能会因被检查的设备的结构材料而异。制药业生产中使用的大约90%的设备都采用不锈钢制成,而其他大部分设备则采用玻璃、橡胶以及特氟龙和EPDM等聚合物材料。
在选择设备和培训检查员时,需要考虑到的一点是聚合物表面上的残留物要比不锈钢设备上的残留物更难以被发现。
尽管如此,暴露在高温下的不锈钢设备可能/将会随着时间的推移而变色,因此相比于设备刚刚交付时,旧设备上的残留物更加难以被发现。如果因为设备表面被划伤而导致无法再安全地验证外观清洁度,则应对设备表面进行重新抛光(如果可能的话)或予以更换。

检查员必须经过相关培训以了解各种表面上各种残留物的外观。

残留物的外观可能会受到不同材料表面的影响(不锈钢对比特氟龙,或者新表面/经过抛光的表面对比变色后的不锈钢表面)。
什么是视觉阈值?
视觉阈值是指API或残留物变得可见的浓度水平。制造商需要确定每种API或残留物的视觉阈值,然后将其与这种API或残留物变得具有毒理学显著性的浓度水平相比较。如果视觉阈值低于您为这种API或清洁残留物预先确定的具有毒理学显著性的浓度水平,则外观清洁可以作为有效的衡量标准。
下面的分析显示了醋氨酚(一种相对低风险的API)变得可见的浓度。
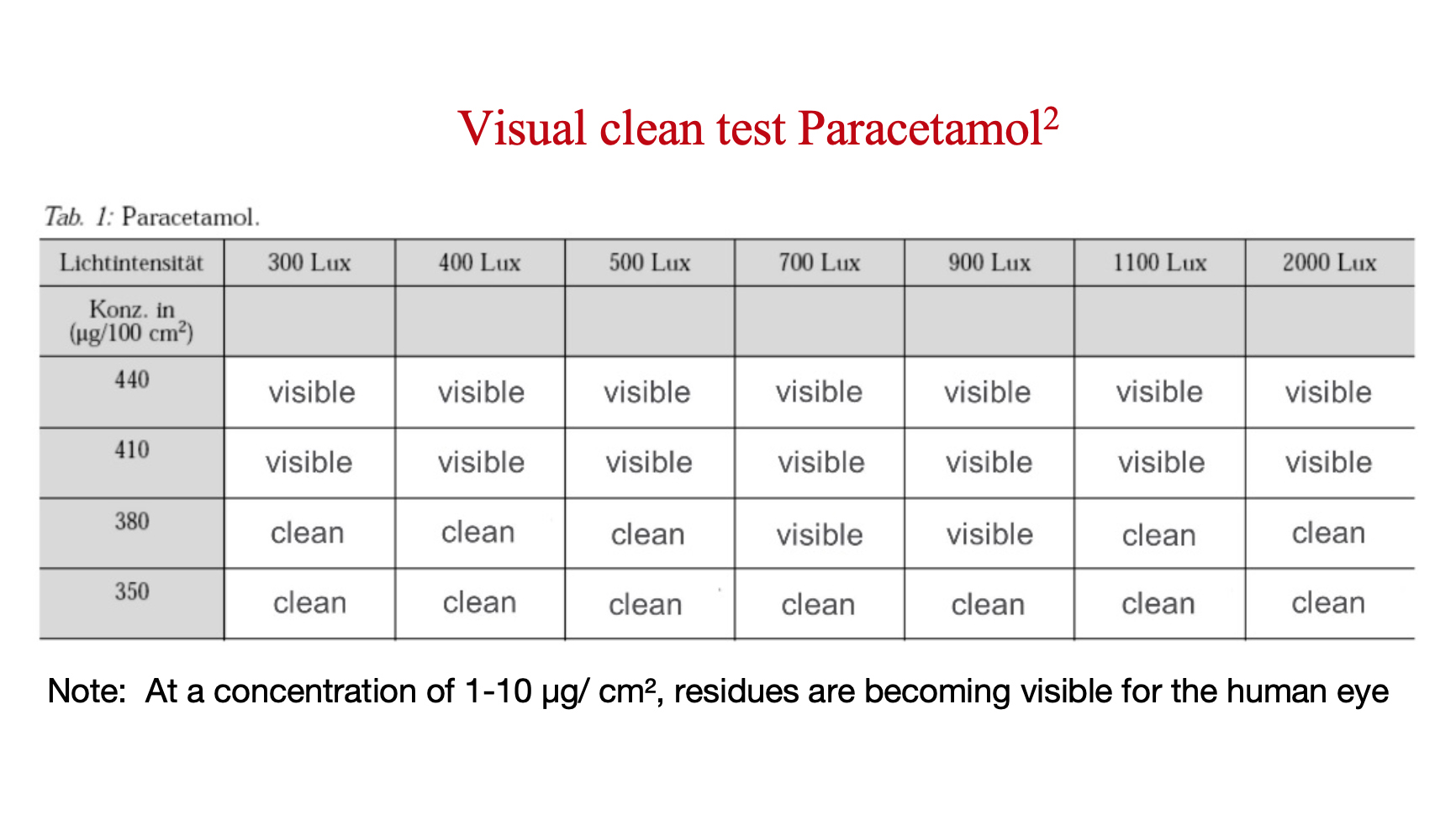
检查员应多久接受一次视力测试?
在这一方面,指导方针同样不够具体。很多公司现在要求从事目视检查的所有操作员每年都必须接受一次眼科检查。
这并非法律要求。另一方面,如果您的清洁程序遭到质疑,请记录下您为检查员提供的全面培训,然后定期测试您的检查员的视力,这样就能够更好地使监管机构相信您已做到了合理预期中您所能做到的一切。
还有其他疑问?
如需了解有关最佳实践和外观清洁指导方针的更多信息,请联系艺康生命科学。我们的身影遍布世界各地的制药场所,因此我们可以带您深入洞察其他制造商如何在其清洁验证程序中执行外观清洁检查。
1FDA - CFR标题21第211.67部分在第(6)点“使用前的设备清洁度检查”中提出了此项要求
2Pharm. Ind. 62, Nr. 6 (2000) Buscalferri et al. − Reinigungsvalidierung


